再生産ソリューションでFDA 510(k)再申請を回避する
形状、適合性、機能、および規制への準拠を維持しながら、医療機器の継続的な生産を確保
顧客の課題
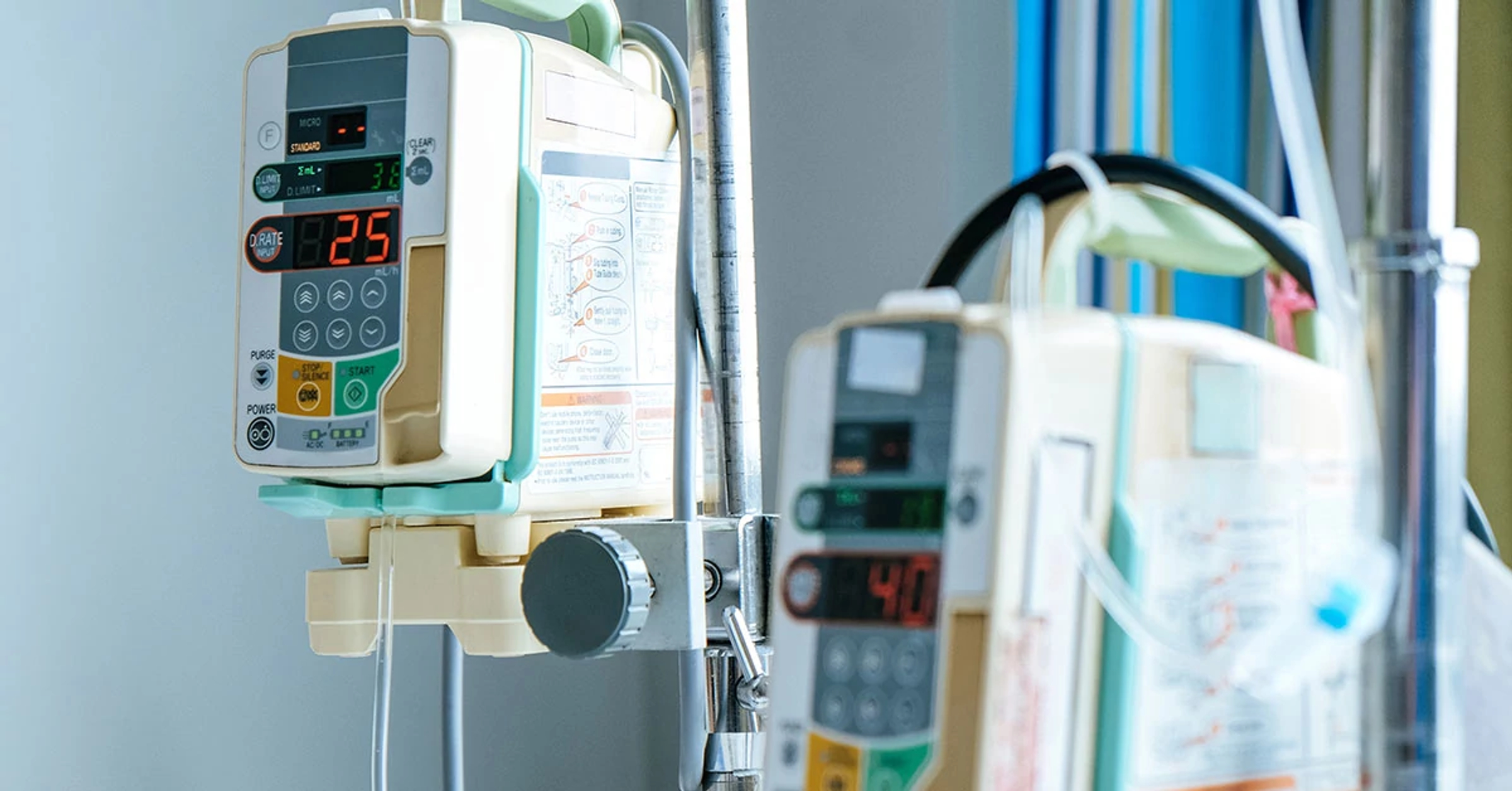
FDAクラスⅡに分類される輸液ポンプシステムを製造する大手医療機器メーカーは、システムのアーキテクチャに不可欠なレガシー製品であるPhilips製8ビット・マイコンの製造中止に伴い、供給面での深刻な課題に直面しました。半導体メーカーによるラストタイムバイの数量は不十分で、正規の製品在庫もすでに枯渇していたため、生産の継続性に即座にリスクが生じる事態となりました。
新しいプロセッサに合わせて輸液ポンプシステムを再設計した場合、以下の対応が必要になります:
- FDA 510(k)の全面的な再申請
- ソフトウェアの全面的な再開発と適合性の再確認
- 数年のわたる検証および適合性評価試験
- 製品供給の中断、多額のコスト、および規制当局による認証の遅延
医療機器メーカーは、規制への適合性を維持し、生産の遅延を回避、そしてコストがかかる再設計を回避できるソリューションを求めていました。
ロチェスターのソリューション
ロチェスターエレクトロニクスとの協業により、この医療機器メーカーは、オリジナルのPhilips製シリコンおよびテストプログラムを用いて再生産された、ロチェスターの8ビット・マイコン数千個を調達しました。この製品は、オリジナルの製品と全く同一のマーキングが施され、形状、適合性、および機能に変更がないことも保証されています。これにより、医療機器メーカーはFDAの新たな510(k)申請を行う必要なく、既存の認証の下で生産を継続することが可能となりました。
FDAのガイダンスに伴い、設計管理手順(21 VFR 820.30)および購買管理(21 CFR 820.50)に準拠した社内検証と文書化のみで対応が可能と判断されました。
すべての検証記録は医療機器メーカーの品質システム内に保管され、安全面および有効性に影響がないことを証明する資料として、いつでもFDAの監査に対応できる状態で保持されています。
その結果、この医療機器メーカーは510(k)の再申請や再設計、そしてソフトウェアの変更を回避でき、生産を一切中断することなく、FDAへの完全な適合性を維持することに成功しました。これにより、稼働中のクラスⅡ医療機器における長期的な生産の継続性が確保されました。
今回の事例は、半導体製品の製造中止に伴うリスクを軽減することで、規制の厳しい長期ライフライクル産業をサポートするロチェスターの能力を改めて示すものとなりました。




